プリオン病の生体に対する作用機序を中心に理解し、その予防法と治療法を把握することにより、 その知識を将来の医療現場に役立てる
プリオン病は、プリオンと命名された蛋白(prion protein)が中枢 神経に蓄積し、神経系を高度に荒廃させ、死に至らせる感染性 の疾患である。 人畜共通感染症として感染予防に関心が持たれている。
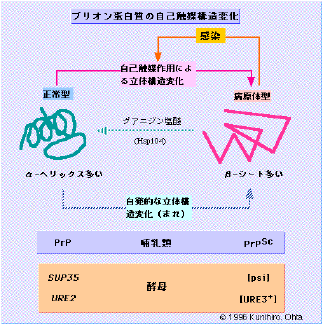
プリオン(Prion)は、proteinaceous infectious proteinの略で、プリオン病の感染 物質としてPruisnerによって名付けられた。感染性があるが細菌、ウイルス などの病原体ではなく、患者の自己蛋白である。ただし、患者の脳に蓄積しているプ リ オン蛋白は、正常の構造とは立体構造が異なるものである。この異常構造のプリオン 蛋 白が体内に入ると、その機序は未だよく判らないが患者の脳にある正常構造のプリ オン蛋白の構造を変え、長い潜伏期を経て発病させるに至る。
簡単に言うと我々の体の中で普通に作られている蛋白質の一つが、変な形に折り 畳まれたものである。第20番染色体に存在するプリオン遺伝子が産生する糖蛋白で あって分子量27000~30000ダルトン。プリオンによる病気は我々の体の部品自体の異 常が病気を生むという点で、ガンによく似ているが、遺伝子自体にはなんら変異がな いことががんと大きく異なる。プリオンを構成する蛋白質ではじめに見つかったもの はPrP(Protease-resistant protein)と呼ばれるものである。最近では、PrP以外に酵 母などにも同じ様な挙動を示す因子が存在することが 明らかにされている。
酵母のpsi及び[URE3]という核外遺伝要素の実体が、実は酵母のプリオンであるこ とが判明した。これらの遺伝子産物の蛋白には、二つのコンフォメーションがあり、 一方が活性型(正常型)で、もう一方が不活性型(病原体型、タンパク質分解酵素に 耐性)である。正常型は通常の細胞機能を持っているが、酵母間の交配(接合とい う)により不活性型蛋白を持つ酵母細胞と細胞質の交換を行うと、不活性型の因子を 鋳型にした蛋白コンフォメーションの変換が起こり、細胞内の大半の酵母プリオン蛋 白質は不活性型になってしまう。このコンフォメーション変化には、折り畳み蛋白質 (シャペロン)という因子の一種であるHSP104が関与しているらしい。興味深いこと に、HSP104を不活性型プリオン蛋白の発現している細胞内で大量発現すると、不活性 型から活性型への回復が起こる。したがって、特定シャペロンの大量投与により、高 等動物のプリオン病を治癒する方法の理論的根拠は存在する。
正常型プリオン蛋白質が、試験管内で病原体型プリオンの存在下、 病原体型の
コンフォメーションに変化することが示された。
プリオン蛋白遺伝子の特定の部位の変異がGSS発症と深くかかわっている。現在
のところGSSの全例でプリオン蛋白遺伝子の変異が明らかになっている。変異の浸
透率も高く、90%以上と報告されている。病理像の特徴は、全症例にプリオン蛋白か
らなるアミロイド斑が認められることで、海綿状態やグリオーシスは症例により違い
がある。マウスを用いた実験的伝達率は低い。
| 表1 日本人GSSにみられるプリオン蛋白遺伝子変異と臨床所見 | ||
|---|---|---|
| 変異部位 | アミノ酸置換 | 初発症状 |
| codon102 | プロリン→ロイシン | 小脳失調症 |
| codon102/219(Lys) | プロリン→ロイシン | 痴呆又は小脳失調症 |
| codon105/129(Val) | プロリン→ロイシン | 痙性四肢麻痺 |
| codon145 | チロシン→stop | 痴呆 |


プリオン蛋白の代謝過程は、培養細胞で研究されており、まずmembrane associated ribosomeで合成されN末のシグナル・ペプチドが除かれ、C末のペプチド もプロセッシングをうけ、GPI アンカーを持つようになる。細胞表面にGPIを有する 分子として存在する過程までは正常型プリオン蛋白の代謝過程であり、それ以後に細 胞内にとりこまれ(エンドゾーム)、リボゾーム等で分解されると考えられている。 一方、異常プリオン蛋白は、この細胞表面の正常プリオン蛋白が細胞内にとりこまれ て後に異常となり、種々の分解酵素に耐性となり細胞内に蓄積する。この結果は、全 てのプリオン蛋白で証明されているのではなく、点変異(codon102)を有するプリオ ン蛋白ではGPIアンカーを受けないことが知られている。さて、ヒトのプリオン病で は野生型プリオン蛋白の場合は異常プリオン蛋白はシナプスに沈着し、codon102変異 では細胞外にアミロイド斑として沈着する。つまりプリオン蛋白の一次構造により、 正常プリオン蛋白のmembrane topologyも異常型プリオン蛋白の沈着部位も異なる可 能性が示唆されている。
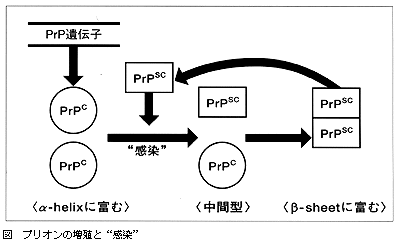
プリオン遺伝子が明らかになって、プリオン遺伝子を破壊したマウス knockout mouse が作られた。このマウスは正常に発育して、いかなる異常も示さない。ところ が、このマウスに病原体型PrPを脳内に接種すると、発病しないことがわかった。こ の実験で分かったことは、PrP遺伝子のノックアウトマウスはPrPを作れず、そのよう な条件では病原体型のPrPは増えないということであった。この実験が基礎になっ て、病原体型PrPが正常型PrPに結合すると、正常型PrPの立体構造が病原体型PrPに 変化して、どんどん殖えるのだという仮説がPrusinerから出された。正常型PrPのα -ヘリックスが、アミノ酸の配列の変化なしでβ-シート構造に変換されると病原性 が出るという。つまり、病原性型プリオンの増殖には正常型プリオンが必要である。 真偽のほどは今後の研究に待たねばならない。
http://riss.narc.affrc.go.jp/seika/data_niah/h06/niah94009.html
最近のプリオン病関連のトピックスとして、”プロテインX”が挙げられるが、日
本では今までこの概念についてほとんど紹介されていない。ここではプロテインXに
関する知見をまとめてみた。
従来、ヒトプリオン蛋白を発現させたトランスジェニックマウスを用いた実験よ
り、PrPSc生成に関与する種特異的な補助因子の存在が推察されてきた。しかし、プ
ロテインXに関する具体的な情報が得られたのはごく最近であり、現在もこれを同定
しようとする試みが精力的に進められている。 さらに、これらの実験結果を治療法
に応用することも試みられている。その主旨はスクレイピー型異常プリオンへの変換
阻害に、我々の同定した変異型プリオン蛋白の有するdominant negative効果を応用
しようというものである。変異型プリオン蛋白を発現させることで、wild typeのプ
リオン蛋白からスクレイピー型異常プリオンへの変換もブロックできる可能性が高い
のである。プロテインXと競合する薬剤をデザインする方法がよいのか、あるいは
dominant negative効果を示す変異型プリオン蛋白を遺伝子操作によって生体内に発
現させる方法のどちらがより有効であるのか、現在トランスジェニックマウス、培養
細胞系を用いた検討が進行している。また、プリオン病に抵抗性のヒツジやウシなど
の種を確立する手段としても、この変異蛋白が応用できる可能性が高い。
自然界では経口感染、胎内感染する。 角膜移植などによって感染した例、成長ホルモンによって感染した例がある。
| ヒト | |
|---|---|
| ヒツジ・ヤギ | スクレイピー |
| オオシカ | 慢性るいそう病 |
| ミンク | 伝達性ミンク脳症 |
| ウシ | 狂牛病(牛海綿状脳症) |
| ネコ・トラ・ピューマ チータ | 猫海綿状脳症 |