緑膿菌
Pseudomonas aeruginosa
G
7 98043 次橋 幸男 98044 坪井 梨江 98045 鶴岡 ななえ98046
富永 直之 98047 戸山 真吾 98049 西 智子
GIO
緑膿菌に関して基礎的な知識から最近のトピックスまで幅広い知識とその検索方法について学び、またグループワークを通じて集団学習の重要性を知る。
SBO
・1
緑膿菌の形態と特徴・2
緑膿菌による病変について・3
細菌学的診断法・4
治療法・5
緑膿菌の多剤耐性獲得機序・6
ムチン産出機序
1
緑膿菌の形態と特徴について
偏性好気性のグラム陰性の桿菌で、シュードモナス科
(Pseudomonadaceae)、シュードモナス属(Pseudomonas)の細菌である。 一般的には、ブドウ糖を嫌気的に分解できないのでブドウ糖非発酵グラム陰性桿菌と呼ばれ、腸内細菌科の細菌とは区別される。 比較的大きな桿菌で、一本の鞭毛を持ち、普通寒天培地などでもよく増殖するが、近年分離される菌は、割と偏平で表面のガサガサした感じのラフ型の集落を作る。 色素産生性があり、臨床分離株ではピオシアニンと呼ばれる緑色の色素とピオベルジンと呼ばれる蛍光色素を産生し、その他にも、オレンジの色素やピンクの色素を産生する株もあるが、年々、色素を産生する株は減少してきており、現在臨床分離の緑膿菌のうち大体50%が色素を産生すると言われている。 緑膿菌という名前は、創傷感染すると、この菌が増殖して傷口から緑色の膿(のう、うみ)が出てくることから付けられた。 学名のaeruginosaも英語の「aeruginous;;緑青色」という言葉に由来する。 緑膿菌とその仲間の細菌は、日本中の病院などで多く使用されているヒビテンなどの消毒薬やある種の化学療法剤に先天的に抵抗性がある。 最近更に薬剤耐性性の細菌が増加しているが、元々自然界にも広く分布し、栄養分の乏しい環境でも生存出来るので、病院などのように感染症の予防や治療の為に消毒薬や化学療法剤を大量に使用している所でも死滅しないで生き残っている。 病原性は余り強くはないが、カテーテルを挿入されている易感染性宿主などでは、カテーテルのチューブにバイオフィルム(biofilm)と呼ばれる膜を被った菌の集落をつくって増殖し、重篤な院内感染や菌交代症、日和見感染を起こす原因となる。 流しや洗面所で、掃除をキチンとしておかないと緑っぽく色が着くのは、多くはこの緑膿菌の繁殖による。 緑膿菌による感染症は、皮膚の化膿、尿路感染症、肺炎などの呼吸器感染症、目の感染や敗血症などがある。
2
緑膿菌による病変について緑膿菌の産出する酵素・毒素
exotoxin A
:重篤な感染症を引き起こす緑膿菌系のものの大半において産出される。ジフテリア菌のように、緑膿菌の
exotoxin Aは、ADPリボシル化を引き起こし、Factor2の伸長の不活性化、タンパク生合成の阻害、細胞死を引き起こす。exotoxin Aは、局所的な細胞死、菌の侵入、そして免疫機能抑制の原因因子である。精製されたexotoxin Aは、マウスに高い致死率を与えており、これはその役割が緑膿菌毒素の主要なものであることを示している。exoenzyme S
:ADP
リボシル化を引き起こすが、exotoxin Aと異なりFactor2以外の部分に働く。この外毒素は肺感染において直接的な組織破壊の原因子であり、菌の拡散にとっても重要なものである。溶血素:
phospholipase C
と rhamnolipidは、脂質とレクチンを分解するために相乗的に働く。両者ともその細胞毒性効果により組織感染に寄与する。. Rhamnolipid(rhamnose―糖脂質を表面に持つ)は、洗剤のような構造を持ち肺サーファクタントのリン脂質を溶かすと信じられており、phospholipase Cによってより分解しやすいようになっている。肺サーファクタントの減少は、慢性・急性の緑膿菌の感染と関係した無気肺の原因となる。Rhamnolipidもまた、粘膜-線毛輸送とヒト呼吸上皮における線毛の機能を阻害する。しかしながら、急性・慢性の感染における相対的なrhamnolipidの役割は知られていない。Protease:
急性緑膿菌感染症の間主要な役割を果たす。緑膿菌は
LasB elastase, LasA elastase, alkaline proteaseを含むいくつかのproteaseを産出する。感染した組織と全身の感染におけるalkaline proteaseの役割は明らかではない。Elastinを破壊する緑膿菌の能力は、急性感染の間は主要な毒性決定因子である。Elastinはヒトの肺組織の主要な役割を担っており、拡張と収縮を引き起こしているものである。さらに、elastinは血球の重要な成分であり、血球の弾性はこれに依存している。関係する2つの酵素、, LasB elastase と LasA elastaseの活性はelastolytic活性によっている。Elastolytic活性は、elastinを分解すると信じられているものである。このelastinはヒトの肺組織に含まれており、緑膿菌の感染による肺出血を引き起こす。LasB elastaseは、亜鉛金属タンパク酵素であり、elastinを含めた多くのタンパクに働く。LasBは緑膿菌のalkaline proteaseの約10倍、カゼインに対するtrypsinの約4倍の活性を持つ高活性の物質である。LasA elastaseは、serine proteaseであり、LasB elastaseと相乗的に働きelastinを分解する。LasA elastaseはelastinを認識し、LasB elastase、alkaline protease、好中球proteaseのような他のproteaseによって分解しやすいように、elastinを過敏な状態とする。LasB elastase も LasA elastaseも共に肺炎の悪化している間中CF(膿庖線維症)の患者の喀痰内に見られる。しかしながら、CFの慢性期における破壊された組織内のLasB elastaseの役割はあまり明らかではない。LasB elastaseはelastinだけでなく、fibrinとcollagenも分解する。また、ヒト免疫グロブリンG、Aのような物質や、気道lysozyme、補足成分、a-1-proteinase inhibitor 、 bronchial mucus(気管支粘膜) proteinase inhibitorのような気管をproteaseから保護する物質なども不活性化できる。それゆえ、LasB elastaseは組織性分を破壊するだけでなく、宿主の防御システムをも妨げる。動物実験による研究で、LasB elastase産出に欠陥のある変異体は、元のものよりも毒性が弱いことが示されている、これはLasB elastaseが毒素としての役割を持つことを支持している。
緑膿菌の病原性
緑膿菌の病原性は低く、健常人に対し感染することは希である。しかし、ガンなどの基礎疾患を持つ免疫不全患者、新生児、老人など
免疫状態が低下した状態の患者の場合、菌株交代の結果として出現し、致死的な感染症を引き起こす。免疫力が低下した患者に対して緑膿菌が強い病原性を示す原因として本菌が、多様な菌体外毒素、菌体外酵素を産出し、宿主の組織・生体防御機構を傷害することが挙げられる。(上記の文章で述べてある)緑膿菌感染による重篤な感染症としては、敗血症が挙げられ、緑膿菌敗血症の場合の致死率は
80%以上といわれている。また、緑膿菌は日本においては50歳前後で発病する進行性のびまん性汎細気管支炎(DPB)における難治性呼吸器感染症の重要な起炎菌でもある。
敗血症
Septicemia:血液
の中で細菌がふえ、全身に感染症をおこしている状態。敗血症の原因には、傷口や手術部位などから直接細菌がはいる場合と、菌血症から進行しておこる場合とがあるが、直接細菌がはいっておこることは少ない。多いのは、すでにかかっていた感染症からすすむ場合である。感染症が悪化すると細菌が血液の中にはいりこむ。これが菌血症で、やがて菌は急にふえだし、循環器系をとおって体じゅうに毒素をまきちらして敗血症がおこる。菌血症は症状があらわれないことが多く、生命にかかわることもないため、敗血症にすすむまで気がつかないことが多い。免疫不全(→ 免疫系)の人に多くみられる。敗血症になると、高熱、寒気などの症状があらわれ、心臓の動きや呼吸がはやくなる。また、白血球の数もふえる。治療せずにほうっておくと、血管内凝固症候群、敗血症性ショック、敗血症症候群がおこり、血圧が一気にさがって、腎臓、心臓、肺などの働きが急にわるくなり、死にいたる。治療は、
抗生物質をもちいるほか、ショックなどの対策も必要になる。
緑膿菌は、
院内感染菌としても重要であるが、病院内での感染はが考えられ、①と②は外因性感染であり、院内感染予防の基本である。
手洗いの励行、消毒の徹底、ハイリスク患者の隔離などを行うことによって院内感染率を低下させることができる。
〈参考文献等〉
戸田新細菌学
http://www.netpassport.or.jp/~wohtsuka/p_aeruginosa/p_ae.htm http://www2.freeweb.ne.jp/%7Emaoda/sepsis.html http://www.ann.hi-ho.ne.jp/a-yuki/sub1/4rui/61(Pseudomonas).htm
3
細胞学的診断法
NAC
培地で分離し、グラム染色、鞭毛染色、オキシダーゼテスト、Hugh-Leifson
培地でOF(酸化発酵)テストを行う。キング培地で色素産出の確認を行う。
4 治療法
ペニシリン系やセフェム系を単独、またはアミノグリコシド剤と併用療法を行う。細菌感受性検査結果を基に選択する。大量投与療法が必要だが、高齢者や腎不全患者が多いので使用量には配慮が必要である。また、カルベニシリンとチカルシリンにはアミノグリコシド剤を不活性化すり作用がある。心内膜炎で弁膜障害を伴った場合、2週間でも治療しなければ、手術が必要になる。慢性気道感染症には、エリスロマイシン少量長期投与(
600mg/日)が有効である。他に、ニューキノロンが使用される。カテーテルが留置されていれば、抜去または入れ替える。
5
緑膿菌の多剤耐性獲得機序はじめに
緑膿菌は多くの抗菌薬に耐性を示す菌種として、古くから臨床的に問題視されてきた。
1980年代に抗緑膿菌薬としてセフスロジン(CFS)、セフタジジム(CAZ)などのβ-ラクタム薬や、イミペネム(IPM)などのカルバペネム、さらに各種のアミカシンなどのアミノグリコシド、シプロフロキサシンなどのフルオロキノロンが開発され、一時的に緑膿菌感染症はコントロール可能のように思われた時期もあった。しかし、これらの薬剤に耐性を示す多剤耐性緑膿菌が、国内外を問わず多くの医療施設から報告されている。わが国でも、多剤耐性緑膿菌が各地の医療施設からしばしば報告されており、院内感染起因菌として注意を払う必要がある。
ⅰ薬剤耐性獲得
緑膿菌はブドウ球菌と並んで抗菌剤に対して高度耐性を獲得しやすい菌種である。薬物の外膜透過性の制限といったん取り込まれた薬物の細胞外排出機構のほか通常の耐性機序であるβ-ラクタマーゼ産生、
PBP(ペニシリン結合蛋白)の変異、アミノ配糖体の化学修飾などが連係して多くの薬剤に対して高度自然耐性が出来上がっていると理解されている。薬物の外膜透過性の制限
グラム陰性菌細胞壁に特有な外膜の透過性が自然耐性と関係している代表的な例である。
Pseudomonas属の菌が多くの抗生物質に示す自然耐性や、グラム陰性菌一般のペニシリンGに対する不感受性は、外膜の孔を薬剤が通過しがたいことに原因があるといわれている。薬物の細胞外排出機構(
efflux pomp)薬剤の菌体内濃度が十分あがらないことが耐性の原因である例は非常に多い。この興味深い例の一つが、能動輸送による薬剤の細胞外への汲み出し
pump outに起因する耐性である。この機構は腸内細菌科におけるプラスミド支配のテトラサイクリン耐性で初めて明らかにされたが、現在緑膿菌をはじめ、多くの菌でその存在が知られている。対象もテトラサイクリン以外の抗生物質、キノロン系合成化学療法剤、消毒剤(アクリジン色素、逆性石鹸)など多岐にわたる。輸送に与かる蛋白の遺伝子はプラスミド性とは限らず、染色体性である例も多い。β‐ラクタマーゼ産出
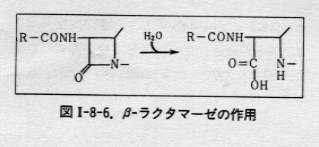
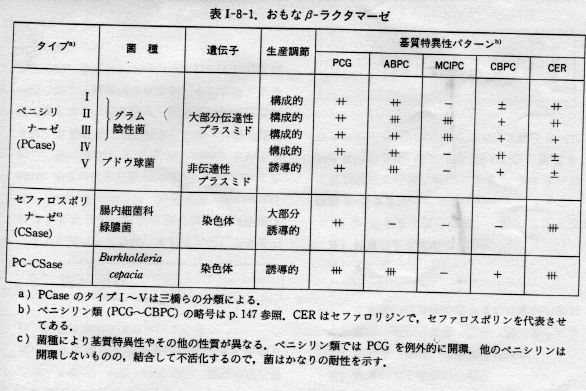
メタロ-β-ラクタマーゼを産生することによりイミペネムなどのカルバペネムに耐性を獲得した緑膿菌は、これまで日本や英国で報告されている。メタロ-β-ラクタマーゼは、通常のβ-ラクタマーゼとは分子遺伝学的に全く異なり、酵素活性の発現に亜鉛原子を必要とする特殊な金属酵素
(メタロエンザイム)であり、ペニシリンからセファマイシン、カルバペネム、β-ラクタマーゼ阻害剤に至るまで、β-ラクタム環構造を持つほとんどすべての薬剤を分解不活化するという憂慮すべき性質を示す。そのため、海外の専門家らも、メタロ-β-ラクタマーゼを産生する緑膿菌やセラチアなどを、今後臨床的に警戒すべき耐性菌として注目している。今回英国で分離された緑膿菌は、ほぼすべての広域β-ラクタム薬(セファマイシン、カルバペネムを含む)に高度耐性を示し、酵素学的な解析からメタロ-β-ラクタマーゼを産生していることが強く示唆された。セフェム、セファマイシン、カルバペネムなどの広域β-ラクタム薬は臨床で用いられている抗菌薬の主流であるため、これらに対し広範かつ高度耐性を示すメタロ-β-ラクタマーゼ産生グラム陰性桿菌の動向に特に警戒する必要がある。
アミノ配糖体の化学修飾
アミノ配糖体アミノ配糖体系抗生物質
(AGs)は、アミノ糖を骨格とする多様な化学構造を示す一群の抗生物質であり、グラム陽性球菌からグラム陰性桿菌にまで、幅広い抗菌活性を示す。
1944年のストレプトマイシンの発見や、それに続く、梅沢らによるカナマイシンの発見と臨床応用は、結核をはじめとする細菌感染症の治療に大きく貢献した。その後、わが国では、1970年に注射用のゲンタマイシン(GM)が認可され、ブドウ球菌や緑膿菌などによる感染症の治療に広く用いられた。GMに耐性を獲得した緑膿菌などが出現する中で、それらが産生する不活化酵素に安定なアミカシン(AMK)が1977年に認可され、さらに、AMK耐性菌の産生する不活化酵素にも安定なイセパマイシン(ISP)が1988年に認可されてきた。一方、メチシリン耐性黄色ブドウ球菌(MRSA)感染症の治療薬としてアルベカシン(ABK)が1990年に認可され、アミノ配糖体系抗生物質は、現在、細菌感染症の治療薬として不可欠な抗菌薬となっている。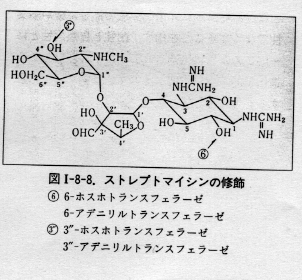
ⅱ細菌間の遺伝子伝達法
緑膿菌は接合及び形質導入により遺伝子を伝達することができる。大腸菌の接合に関係する
F因子に対応して緑膿菌ではFP因子と呼ぶ。遺伝子地図もかなり明らかになっている。R-プラスミドも多数見つかっている。従って薬剤耐性を獲得した緑膿菌は、耐性を持たない周囲の緑膿菌に対して耐性をコードした遺伝子を伝達し耐性を獲得させることができると考えられる。外来性の耐性遺伝子の大部分は薬剤耐性プラスミドに担われている。グラム陰性菌である緑膿菌の
Rプラスミドは接合伝達能があり、また薬剤耐性プラスミドには複数の耐性遺伝子を保有するいわゆる多剤耐性プラスミドが少なくない。
参考文献
「戸田新細菌学」感染症情報センター
http://idsc.nih.go.jp/index-j.html
6
ムチン産生の機序
細菌バイオフィ
ルムは、本来、細菌が環境に順応して生き延びて行くために形成する細菌集落のありかたの一つであって、細菌自らが分泌す る粘性の多糖類と菌体とからなる構造体である。人間の体内で、感染という形で侵入した病原菌によって形成されるバイオフィルムは結果的に抗菌剤や生体の防禦機構から病 原菌を護るように作用し、感染症からの回復を妨げる。緑膿菌はバイオフィルムを形成することにより、しば しば難治性の呼吸器感染症や尿路感染症の原因となる。緑膿菌が 産生する多糖類はアルギン酸であり、構造や合成経路、産生の制御機構などについて非常に良く研究されている。
A.
バイオフィルムとは
細菌の場合は浮遊状態でも生きてはいけるが、何かの表
面で集落を形成して生存の場とすることが多い。そのような場合、細菌はまず水中で何かの表面に付着しなければならない。付着(adhesion)はまず静電的要素による可逆的な吸着 (association)に始まり、次いで細菌によってそれぞれ異なる固有の付着因子(adhesin)による非可逆的な状態へと移行する。付着した細菌は種々の多糖体(exopolysaccharide; glycocalyx ともいう。また slime という場合もあるが、これは、菌が細胞外に分泌した多糖体やタンパク質、あるいは核酸成分の混合体を指すことが多い)を菌体外に分泌しながら分裂をくり返し、小 集落(microcolony)を形成して行く。すなわち、小集落は、 菌体が多糖体の層の中に埋め込まれた状態で形成される。このような小集 落は成長しながら合体していき、細菌にとっての生活域(matrix) を形成するが、このような matrix をバイオフィルムと総称する。
人体の中でも、細菌は歯の表面などにバイオフィルムを作ることにより常在細菌叢を構築するが、このような場合にはヒトと細菌は共棲関係を維持することが出来る。しかし、病原性
細菌による人体内でのバイオフィルム形成は重大な問題となる。体内でのバイオフィルム形成には細菌が分泌する多糖体以外にも、宿主由来のフィ ブロネクチン(fibronectin)、血液細胞、その他が関与し、自然界に.存在するよりも複雑な構造体を形成する。感染の場で菌がバイオフィルムを形成すると、菌は多糖体やその他の宿主由来の成分の中に埋め込まれた状態になるが、このよう な菌は本来感受性を有する抗生物質やその他の抗菌剤から物理的に保護されることになり、また、膜構造にも何等かの変化を おこし、これら抗菌剤に抵抗性になる。
生体は侵入する細菌などの異物に対して、常に好中球やマ
クロファージ(macrophage)と言った、いわゆる貪食細胞で対抗し、これら異物を貪食、消化、排除している。このような貪食 細胞の働きは生体の防禦機構の極一部を担うにすぎないものではあるが、細菌の侵入と組織への定着を阻止するという意味で 極めて重要である。「感染」とは、生体の防禦機構、特に貪食細胞による排除機構が細菌の侵入、増殖を防ぎきれなくなった状 態であるが、「感染」後においても貪食細胞は感染菌に対して果敢な戦闘を続けることになる。抗生物質を始めとした抗菌剤を 投与することにより、感染菌の大部分は殺すことが出来るが、生体の防禦機構の援護なしで完治に導くことはほとんど不可能と考えられている。バイオフィルム菌は、このような貪食細胞に よる貪食、殺菌作用にも抵抗性になるという点でさらにやっかいなものとなる。
B.
細菌が分泌する多糖体とは
一般に、化膿性の気管支炎が長期間持続し、広範な細気管支の壊死から気管の壊死に至る。この病気にかかった人々の多くはムコイド型の緑膿菌
(Pseudomonas aeruginosa)による肺の感染症で死亡する。ムコイド型緑膿菌は非ムコイド(mucoid) 型のものと比較して、より多くの多糖体を菌体外に分泌する。我 が国でも見られる呼吸器病に彌慢性凡細気管支炎(diffuse pan-bronchiolitis)というものがあるが、この感染症の主たる起炎菌 もまた緑膿菌である。これらの感染症は極めて難治性であるが、その原因として細菌が分泌する多糖体の存在が考えられている。 それゆえ、これら多糖体の性質や生合成経路、遺伝子学に関する研究が成されている。
緑膿菌、特にムコイド型緑膿菌、が産生する多糖体はアル
ギン酸(alginic acid、 alginate)である。アルギン酸は緑膿菌以外のある種の細菌によっても産生されるが、他に海の種々の藻類によっても産生される。D-マンヌロン酸(D-mannuronic acid、D-mannuronate)とこのものの C-5 epimer である L-グルロン酸(L-guluronic acid、L-guluronate)とが β-1,4 結合で直線的に繋がった copolymer であるが、緑膿菌のアルギン酸は、マンヌロン酸のO-2 もしくは稀ではあるが O-3 または両方の位置でO-アセチル基によって修飾されている点で、藻類のそれとは異なっている。緑膿菌のアルギン酸は、他由来のアルギン酸とくらべ粘性が高く、これはグルロン 酸の量比がより少ないことに起因していると考えられている。さらに、濾胞性肺腺維症の患者の肺内で特に高レベルで存在するCa2+が緑膿菌の産生するアルギン酸のマンヌロン酸/グルロ ン酸比を制御している、すなわちグルロン酸比を減少させているのではないかと考えている研究者もいる。つまり、これ らの患者の肺内で病巣を形成する緑膿菌は、高濃度の Ca2+の影響でグルロン酸比の少ない極めて粘性の高いアルギン酸を産生 し、それゆえ抗菌剤や生体防禦機構の影響をさらに受け難くなるというのである。事実、カルシウムイオンはアルギン酸ゲル を安定化し、ムコイド型緑膿菌集落をより固いものにすることが知られているし、また、金属イオンのキレート剤である EDTA が in vivo で緑膿菌感染に対する抗生剤の効果を高めることも報告されている。
緑膿菌のアルギン酸生合成経路については、
Lin and Hassidによる褐藻、Fucus gardneri、 のアルギン酸生合成経路の研究と、Pindar and Bucke(による細菌、Azotobacter vinelandii、 での研究の成果から明らかになってきた。現在提唱されている合成経路を図1) に示した。緑膿菌のアルギン酸合成の最初のプリカーサーはフラクトース 6-リン酸(fructose 6-phosphate (F6P))である。F6P は リン酸マンノース異性化酵素(phosphomannose isomerase (PMI))とリン酸マンノース転移酵素(phosphomannomutase (PMM))によってマンノース 6-リン酸(mannose 6-phosphate (M6P))を経てマンノース 1-リン酸(mannose 1-phosphate (M1P))に導かれる。 M1P は、次に GDP-マンノースピロ加リン酸分解酵素(GDP-mannose pyropho-sphorylase (GMP))と GDP-マンノース脱水素酵素(GDP-mannose dehydrogenase (GMD))の作用を受けて GDP-マンノースから GDP-マンヌロン酸へと移行する。GDP-マンヌロン酸は、さらに重合(polymerization)、アセチル化、エピメリ化を受けた(順序は不明)後分泌されるが、これらの過程につ いてはよく分かっていない。
図
. 1. アルギン酸生合成経路矢印1,2,3,4は重合、アセチル化、
export、エチメル化の不明瞭な段階を示す。各々の酵素がコードされてるゲノムは酵素名の上に示す。アルギン酸の化学平衡はPMI,GMPにより、それは化学反応のすすむ矢印の方向が相対的であることによって示唆される。 F6P, フラクトース 6-リン酸;M6P, マンノース 6-リン酸;M1P, マンノース 1-リン酸;GDPM, GDP-マンノース;GDPMA, GDP-マンヌロン酸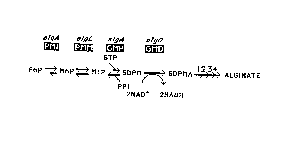
参考文献等;
http://www.glycoforum.gr.jp/science/word/glycoprotein/GPA06J.html http://www.gak.co.jp/TIGG/TIGG44/44MR3j.html#fig1
参考文献
Christian Van Delden and Barbara H. Iglewski
University of Rochester School of Medicine and Dentistry, Rochester, NewYork, USA
http://www.cdc.gov/ncidod/eid/vol4no4/vandelden.htm