肺炎クラミジアと心臓血管疾患
肺炎クラミジアは、急性呼吸器疾患を引き起こす偏性病原体である。肺炎クラミジア感染のスペクトルは、アテローム性動脈硬化とその臨床徴候、血清疫学的な研究によって、肺炎クラミジア抗体が冠状動脈疾患、心筋梗塞、頸動脈疾患、脳血管疾患と関連づけられてきた。肺炎クラミジアのアテローム性動脈硬化症との関連は、アテローム性動脈硬化病変組織中には動脈
treeを通して存在し、健康体の動脈組織中にはほとんど存在しないことによって確証されている。肺炎クラミジアは、同様に冠状血管や頸動脈アテローム性班からも単離されている。慢性感染が疾患の惹起や進行に役割を果たしているかどうかを決定するため、ヒトの介入研究が始められ、肺炎感染動物をモデルにした研究もさらにすすめられた。このレビューは、心臓血管疾患における肺クラミジアの関連性と、潜在的役割について証拠をまとめたものである。肺炎クラミジアは、ヒトの呼吸器疾患を一般に引き起こす原因であるが、初めて1965年に台湾である1人の子供の結膜から分離された。その後、1983年ワシントン大学で大学の生徒の咽頭から分離されたとき、主要な呼吸器系病原体として、認められた。肺炎クラミジアは、おおよそ地区肺炎の40%、咽頭炎、気管支炎や副鼻腔炎の5%を引き起こしている。肺炎クラミジアの肺感染の臨床的症状はいくつかの区別できる特徴を除いて、他の呼吸系病原体によって引き起こされる症状と類似している。亜急性の開始と咽頭炎は共通である。しばしば、二層性のパターンが見られ、咽頭炎は気管支炎や肺炎の進行前におさまる。咳は共通で長引く。肺炎は相対的に軽症だが、抗生物質療法によってさえ、回復後は遅く、咳と倦怠感が何週間にもわたって続く。肺炎クラミジア感染の疫学について考慮すべき知見が、肺炎クラミジアに特有のマイクロ免疫蛍光テストによって導き出された。肺炎クラミジア感染は偏在性なのである。事実、誰もが人生のどこかで感染し、再感染も一般に起こる。肺炎クラミジア抗体は5歳以下の子供には稀であるが、発展途上国と熱帯の国は例外である。抗体保有率は5歳から14歳にかけて急速に増加し、20歳では50歳に達する。その後、60歳から70歳で70~80%にゆっくりと増加を続ける。肺炎クラミジアは他の急性や慢性の呼吸器疾患(例えば、中耳炎、慢性閉塞性肺疾患、肺嚢胞性線維症の再燃・喘息)や、他の臨床症状(例えば、結節性紅斑、
reiter症候群サルコイドーシス)と関連があるとされてきた。これらの関連性は血清疫学的な観察、ケース報告、生体からの単離・直接検出、抗クラミジア抗生物質の反応やこれらのメソッドの組み合わせによって決定された。肺炎クラミジア感染の広範囲なスペクトルはアテローム性動脈硬化症状や、関係のある冠状動脈疾患や頸動脈狭窄、大動脈瘤、四肢の動脈閉塞や発作などの臨床症状にまで拡がっている。
この概要は、アテローム性動脈硬化症を肺炎クラミジア感染と関連づける研究をまとめ、原因役割のもっともらしさを示唆する予備的な
in vitroとin vivo研究が討議されている。(ここまで東史子訳)
<アテローム硬化型の組織の中に肺炎クラミジア菌は存在するか?>
冠動脈疾患の患者は、肺炎クラミジア菌に過去に感染した血清学的証拠を持つ傾向にある。肺炎クラミジア菌リポ多糖を含む免疫の複合もまた
42-and48-kDaの肺炎クラミジア菌の特異的な抗体と関係している。これらの関係は立証され、頚動脈疾患や脳血管疾患に拡張する。集団のなかで肺炎クラミジア菌抗体の流行がケースとコントロールの統計学的に有意な違いを示すとは考えられないが、血清免疫学の研究が一貫した関係を見出した。肺炎クラミジア菌抗体は18の研究において肝血管心疾患と脳血管疾患に関係している。)ほとんどは2.0もしくはそれ以上のオッズ比をもっていた。ほとんどは統計学的に有意でその危険性は他のアテローム性動脈硬化症の危険因子とは無関係である(すなわち高コレステロール血症、喫煙、高血圧症、糖尿病、家族歴など)。2700人の患者と5000のコントロールの研究は肺炎クラミジア菌抗体と循環器疾患の血清学的関係を示した。肺炎クラミジア菌とアテローム性動脈硬化症の関係の証拠はポリメラ-ゼ連鎖反応法、免疫細胞化学的染色、電子顕微鏡によって得られてきたアテローム性肝血管に見られる構造が肺炎クラミジア菌の形態学的特徴に著しく似通っているという事実によって明らかになった。肺炎クラミジア菌固有の単クローン抗体を使った
ICC染色によって、肺炎クラミジア菌は7組織中5組織のアテローム硬化型病変において見出された。PCRまたはICC染色によって36の剖検(組織を取り出すこと)された冠動脈組織中20において有機体が発見された。ワシントンの大学において、その有機体は染色と繊維性脂肪斑における肝血管、頚動脈、大動脈、大腿・膝窩のアテロームにおいて発見された。ICC染色を用いたすべての研究において、コントロール組織が背景となる染色を除外するためにコントロール抗体で染色された。その有機体は異なる年齢や民族である男女の研究参加者の組織において発見された。他の調査員はこれらのことを確認しており、腸骨動脈や腹大動脈瘤や大動脈狭窄の組織におけるアテローム硬化型病変の有機体もまた発見した。その有機体は497の組織標本中257(52%)のアテローム硬化型病変において発見された。対照的にその有機体は正常組織のたった2%にしか見られなかった。正常な動脈組織に比べ、病気を持った動脈組織は10のオッズ比を示している。われわれの研究においてその有機体は組織学的に正常に見える心血管組織においては発見されなかった。(
ここまで原崎加奈子訳)
|
Table. Studies of Chlamydia pneumoniae in atherosclerotic tissue
|
|||||
Source of specimens |
Artery |
Type of specimen |
Atherosclerotic |
||
|
|
|||||
|
South Africa (7) |
Coronary | Autopsy 20/36 (56) | 20/36 (56) | ||
| PDAYb study (8) | Coronary | Autopsy | 8/18 (44) | ||
| Univ. Washington (9) | Coronary | Atherectomy | 20/38 (53) | ||
| Alaskan Natives (10) | Coronary | Autopsy | 23/59 (39) | ||
| Louisville, Kentucky (11) | Coronary | Vascular surgery | 7/12 (58) | ||
| Japan (12) | Coronary | Atherectomy | 20/29 (69) | ||
| Salt Lake City, Utah (13) | Coronary | Atherectomy | 71/90 (79) | ||
| India (14) | Coronary | Coronary artery bypass | 4/40 (10) | ||
| California & Univ. Washington (15) | Carotid | Endarterectomy | 37/61 (61) | ||
| Germany (16) | Carotid | Endarterectomy | 7/50 (14) | ||
| Canada (17 ) | Carotid | Endarerectomy | 54/76 (71) | ||
| Univ. Washington (18) | Aorta | Autopsy | 7/21 (33) | ||
| Finland (19) | Aorta | Vascular surgery | 12/12 (100) | ||
| Italy (20) | Aorta | Vascular surgery | 26/51 (51) | ||
| United Kingdom (21) | Aorta, femoral, iliac | Vascular surgery | 15/33 (45) | ||
| California (22) | Popliteal femoral | Vascular bypass | 10/23 (43) | ||
| Finland (23) | Aortic valve | Autopsy | 25/46 (54) | ||
| Sweden (24) | Aortic Valve | Surgery | 19/39 (49) | ||
|
|
|||||
|
aNumber positive by immunocytochemical staining and/or polymerase chain reaction over number tested. |
|||||
|
|
|
Figure 1. Ultrastructural evidence of Chlamydia pneumoniae in coronary atheroma. This transmission electron micrograph demonstrates the presence of endosomes containing C. pneumoniae pear-shaped elementary bodies within a foam cell in tissue from coronary artery atheroma. Arrows in inset point to the elementary bodies. Bar=0.5オm. (Reprinted from Journal of Infectious Diseases (8) with permission from the publisher, University of Chicago Press). |
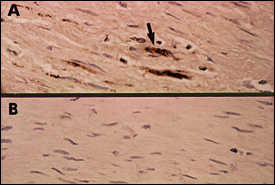
Figure 2. Immunocytochemical staining demonstrating Chlamydia pneumoniae in fibrolipid plaque from coronary artery atheroma. Panel A illustrates positive staining of foam cells in the plaque with the C. pneumoniae—specific monoclonal antibody TT-401. Panel B shows negative staining of the adjacent section using normal ascites fluid as the control. |
肺炎クラミジアを、アテローム性の組織から単離するのは困難であった。慢性のクラミジア感染組織、反復して接種された実験動物からの単離が稀であることから考えると、驚くべきことではない。しかし、その生物(肺炎クラミジア?)はしばしば、
DNAおよび抗原検出法と、慢性の炎症反応によって示される。アテローム性動脈硬化症の免疫学的特徴は、慢性感染に起因する炎症反応に似ている。最近の2つのケースでは、肺炎クラミジアは、アテローム性のプラークから単離された。最初の単離は、多施設治療の間に得られた。多施設治療は、心臓移植を受けた患者(冠状動脈の疾病を持つもの、あるいは持たないもの)の冠状動脈に施された。その生物は。アテローム性動脈硬化症の患者の、10人に7人に発見された。すなわち、それは、冠状動脈にあとのなかった二人の患者においては発見されなかったということを示している。肺炎クラミジアは、冠動脈の重い疾病を抱えた患者の、アテローム効果型病変から単離された。次の単離は、シアトルで、頚動脈内膜切除を受けた患者の頚動脈アテロームの検査から得られた。肺炎クラミジアは、
16の標本のうち11から検出され、頚動脈内膜切除を選択して受けた患者から、培養された。肺炎クラミジアに加えて、他のもの、単純ヘルペスウイルス(
HSV)やサイトメガロウイルス(CMV)、ヘリコバクター=ピロリが循環器病に関係する。2、3の検査のみが、肺炎クラミジアとこれらの伝染性の生物体と同時発生的に研究された。若者のアテローム動脈硬化症を考慮すると、アテロームの7例中6例と、内膜肥厚の11例中2例が肺炎クラミジア陽性であった。すなわち、影響を受けない31組織全てが陰性であったということである。アテロームの2例と、正常組織の2例は、CMV陽性であった。ただ1つの冠状動脈アテロームが、CMVと肺炎クラミジア双方に要請であった。頚動脈のアテローム性動脈硬化症における肺炎クラミジア、CMV、HSVの存在の発見を考慮すると、肺炎クラミジアも。CMV(35%)とHSV(10%)よりももっと頻繁に発見された。(75%)このうち2つか3つに感染していたのはそれぞれ、23.7%と7.9%であった。肺炎クラミジアとCMVはそれぞれ独立して、血栓症の危険増加に関連していた。大動脈瘤における、肺炎クラミジア、あるいはヘリコバクター=ピロリ、あるいはその両方の存在を考慮すると、51人中47人の患者がヘリコバクター=ピロリに血清陽性だったという事実にもかかわらず、この生物体は、アテローム硬化型のプラークのな化に発見されなかった。このように、肺炎クラミジアはもっと頻繁に、単に伝染性生物体として発見される。
<肺炎クラミジアはアテローム発生に一役かっているか?>
肺炎クラミジアはアテローム硬化型の病変に存在するというしっかりとした証拠があるにもかかわらず、その生物体の存在が、疾病の病理発生に関係があるという証拠は、偶然性による。
3つの可能性が考えられる。その生物体は、1)血管の細胞を統括するが、病理的異常性を与えない。2)初期の傷害の原因となり、アテローム硬化型の過程を引き起こす、3)その疾病の重症度を高めるか進行を早めるかする。(
ここまで原田真生子訳)もし、肺炎クラミジアが関係するとすれば、その役割はアテローム発生のイベントの前後関係を適応させることに違いない。その病変発生の初期に起こる内皮の損傷もしくは活性化などよって、内皮への単球/マクロファージの粘着、内皮下層からの遊離、それらを泡沫細胞に変化させる酸化した低密度リポタンパクの取り込み、そしてサイトカイネ-スの遊離が起こる。それらのサイトカイネ-スは白血球接着の増加を導く内皮細胞接着分子を上方制御する。内皮の損傷部位における血小板凝集は、平滑筋細胞の増殖を刺激する血小板由来成長因子の遊離を引き起こす。脱分化した平滑筋細胞は、線維性組織の形成を導くコラーゲン、エラスチン、そしてプロテオグリカンを分泌する。成熟フィブロリィピット(線維脂肪)はマトリックス成分から成る線維性キャップによって囲まれた脂質/コレステロール-リッチ
コアにより構成される。ヒトの組織研究
肺炎クラミジアは「無害な傍観者」である、という仮説について研究されている。ある研究では、クラミジアが解剖的に異なる部位の組織からどれくらいの頻度で発見されるかについて調査した。38人の患者の死体解剖で、冠状動脈、肺、肝臓、脾臓、そして骨髄を含む組織でクラミジアが発見された。38人中半分の人に死ぬ以前に心臓血管の疾病が認められた。21人の患者に1つもしくは多数の組織に肺炎クラミジアが認められた。心血管にクラミジアが発見されたのは、18人で(うち11人は心血管組織のみで)あった。そして、心血管とそれ以外の組織の両方にクラミジアが発見されたのは7人であった。肺炎クラミジアの保因者3人のうち、2人は肺組織のみに、1人は脾臓のみにクラミジアが発見された。この研究から心血管以外の組織でも肺炎クラミジアがみられること、そして心血管組織では非常に頻繁にクラミジアが発見されることがわかった。
アテロームにおける頻繁な肺炎クラミジアの存在についての別の可能な説明として、感染した肺のマクロファージがクラミジアをどの肉芽腫性組織にも広める、というものがある。結核、ライ病、コクシジウム病、クローン病、リウマチ様小結節、巨細胞腫瘍、もしくはサルコイド-シスの患者からえた外科的もしくは解剖学的な肉芽腫の標本33個のうち3つに肺炎クラミジア、全てにサルコイド皮膚肉芽腫が含まれていた。サルコイド-シスは肺炎クラミジアについての血清学会合で未知の病因として報告された病気である。これらの研究は、アテロームには肺炎クラミジアが感染した肺細胞が優先的に(高頻度に)発見されることを示唆する。
In
Vitroにおける研究動物モデルとヒトにおける観察と一致した、試験管内の研究は、血管の細胞は肺炎クラミジアに感受性をもつこと、そして、アテローム性動脈硬化症のキー(
key)細胞である、ヒトのマクロファージ、内皮細胞、そして平滑筋細胞における肺炎クラミジアの生産的感染について論証した。また、試験管内の研究は、感染が免疫調節の産生を導くかどうかについても調査した。一次宿主細胞は気管と上咽頭を裏打ちする上皮細胞である。まず、試験管内でアテローム発生における肺炎クラミジアの潜在的な役割について取り組み、低密度リポタンパク質の付加によって起こる肺炎クラミジアに対するヒトの単球由来のマクロファージは、泡沫細胞形成とコレステリルエステルの蓄積の原因となることがわかった。泡沫細胞の形成はアテローム硬化の過程の初期に起こる。超微細構造の研究は、クラミジア特異的で細胞特異的
MABsをつかった二重のICC染色によって、肺炎クラミジアは大動脈のアテローム障害のある部位の平滑筋細胞とマクロファージの両方から発見し、マウスの繊毛性気管支細胞、マウスとウサギの肺マクロファージ、そしてヒトの泡沫細胞(マクロファージ)と脂肪を吸収した平滑筋細胞における肺炎クラミジアについて明らかにした。同様に、症候性冠動脈病の患者からとった標本で、粥腫切除組織のマクロファージ中に肺炎クラミジアが発見され、また、粥腫切除、肺炎クラミジア菌血症から得た組織のPCR陽性のバフィーコート標本にも発見された。症候性冠血管アテローム性動脈硬化症の患者では、その13%にクラミジアが発見された。コントロール標本では発見されなかった。肺炎クラミジア感染のモデルマウスでは、肺炎クラミジアが抹消血の単核細胞の培養とPCRでは見られたが、鼻腔内接種した血漿には見られなかった。炎症誘発と凝血原活動の産生を誘発する肺炎クラミジア感染能は、アテローム硬化の過程の一貫した免疫反応を引き出す上でのその推定上の役割を決定することが研究された。ヒトの血管内皮細胞の肺炎クラミジア感染は、組織因子の産生、単球走化性タンパク-1のレベルの増加、そして感染した細胞に対する血小板接着の増加を引き起こす。内皮細胞における感染もまた、白血球接着に重要なセレクチン、細胞接着分子-1、そして血管性接着分子-1を含む接着分子の発現を引き起こす。最後に、マクロファージにおける感染は炎症誘発性サイトカイン、腫瘍壊死因子α、インターロイキン-1β、インターロイキン-6、そしてインターロイキン-8の産生、同様に
cd14分子の発現を引き起こす。(
ここまで原田慶美訳)動物のモデル
研究はアテローム発生の肺炎クラミジアとなる潜在的な可能性をもつということを支持しているが、病因学は動物のモデルや介入の研究によってのみ確立するものである。ウサギとマウスは肺炎クラミジアに感染しやすくアテローム性動脈硬化症のよいモデルとなる。どちらの種での呼吸器疾患も多層性間質性肺炎によって特徴づけられる。この病気はマウスのほうがシビアで長く続き、肺や大動脈から容易に単離される。
ウサギのモデルはクラミジア肺炎の呼吸器感染が血管壁感染とアテローム性動脈硬化症に特徴的な炎症性の変化を導くかどうかを決めるのに使われてきた。ある研究ではニュージーランド色ウサギが1ヶ月で肺炎クラミジラの鼻咽頭の感染を受けた。10匹の2匹のウサギはアテローム硬化性の変化を示した。その変化は菌の植え付け後7日目と14日目に観察された。
1
匹のウサギは大動脈弓に気泡細胞の蓄積があり(これは早い病変に特徴的である)、腹大動脈に局所的な動脈の炎症が認められた。2番目のウサギでは大動脈の平滑筋内に金紡錘細胞の増殖が見られた。どちらのウサギも細気管支炎と間質性肺炎となっていた。別の研究ではアテローム硬化性のような変化が肺炎クラミジアの植え付けを受けた後2~4週間で9匹のうちの7匹のニュージーランド白ウサギの大動脈で見つかった。どちらの研究においても、ウサギは普通の食事を与えられ、コントロールのグループにはアテローム硬化症は見られなかった。われわれは
C57BL/6Jのマウスとアポリポタンパク質Eのノックアウトのマウス(以下アポE)を使い、上気道の感染、つまり肺のマクロファージの感染が大動脈に撒き散らされ、アテローム性動脈硬化症発生に関与しているという仮説をテストしようとした。アポEの背景の血統であるC57BL/6Jのマウスは脂肪とコレステロールの高い食事を与えられたときのみにアテローム性動脈硬化症となった。それとは対照的にアポEのマウスは時間と年齢による方法で普通の固形資料を与えられて自然に、人間の病気のいくつかの特質とともにアテローム性動脈硬化症の病変となった。我々はC57Bl/6Jのマウスを使い、鼻腔内や腹腔内の感染の後には肺炎クラミジアが肺胞と腹膜のマクロファージにそれぞれ感染することを明らかにした。それに加え、組織が血漿中にはなく血液の単核白血球に見つかったことから、細胞に関係した菌血症が急な感染に続いておこったということがわかった。肺炎クラミジアを鼻腔や腹腔に植え付けたマウスから得られた肺胞や腹膜のマクロファージを腹腔内に植え付けたことによる菌の移動は、結果として肺・胸腺・膵臓・腹腔リンパ腺へと感染を撒き散らすことになる。感染は大動脈へ菌を散布することになるかということと、さらに感染が人の病のようにアテローム硬化症の病変の中に見られるかということを知るために、アポEのマウスは単一、あるいは多数の菌の鼻腔内への菌の植え付けを受けた。肺炎クラミジアは大動脈への感染後20週までに、ICC染色により見かけ上は気泡細胞となっている病変部の中に発見された。大動脈が陽性の時は肺炎クラミジア陽性のマウスの割合は33%~100%であった。コントロールは肺炎クラミジアに陰性のままであった。対照的に背景血統(
C57BL6/J)の12匹の動物のうち1匹(0.8%)で動脈にアテロームを起こすものが入っていない食事を与えられたものは感染から2週間までは(しかしそれ以降ではない)大動脈にその組織を含んでいた。人の肉芽腫性組織や様々な解剖的な場所の研究のように、これらの研究は組織中にはアテローム硬化型病変への向性があるということを示している。コンピューターに補助された病変サイズの分析は肺炎クラミジア感染が病気の進行具合を変えるかどうかを決めるのに使われてきた。肺炎クラミジアの鼻腔内感染を次の3回の異なる時間にした10匹の感染したマウスと10匹の感染していないマウスの比較により、感染は有意に病変サイズの進行を早めていることがわかった。このようにウサギとマウスモデルの昔の研究により、肺炎クラミジアはアテローム硬化性のものと同様な炎症性の変化を誘発しアテローム硬化型病変の進行をはやめることがわかった。
<粘り強い感染>
肺炎の抗体とDNAはしばしばアテロームに見られるが、単離はまれである。同様に肺炎クラミジア感染のマウスのモデルでも、肺はPCR反応が陽性でありつづけ、病変は組織がそれ以上培養できなくなったあとも持続した。アポEモデルでも、感染後
3週間までは少しのマウスでは肺や大動脈から組織は培養できるが、感染後20週まではPCR反応とICCがどちらの場所でも探知できる。培養が陽性の非存在下でPCR陽性は持続性感染や退化しないDNAを表しますか?二つの証拠のラインが強く生存可能な組織の存在を支持している。二つの異なる血統のマウスを使った二つの独立の実験は肺の感染はコルチゾンを含んだ処置によって復活することを示している。とくに鼻腔内接種の後で、組織がそれ以上肺から培養されないとき。動物はコルチゾンかセリンとともに処置された。セリンとともに治療すると、PCR反応は頻繁に陽性でも、肺炎クラミジアは培養されない。反対にコルチゾンで処置すると、感染したマウスの46%と60%の確率で、復活した感染が明示される。二つ目の証拠のラインは生きていてUVに不活性となった組織とともに急に鼻腔に感染したマウスからきた。:肺胞のマクロファージは感染後何回か孤立した。生きている組織が使われたときは、その組織は培養され、感染後7日まではPCRによって探知される。対照的にマウスがUVに不活性化された組織とともに植え付けられたならば、その組織は孤立したマクロファージが植え付け後即座にPCRによってのみ探知される。これらの実験により死んだ組織からのDNAは急速に退化して、それに対し生きている組織はマクロファージの中で生存する。(ここまで原一生訳)
クラミジア感染が抗生物質投与の後に持続することがあるということは
, 動物のモデルにおける人間へのクラミジアの薬剤効力の研究は警告で解釈されるべきだ。 2つの抗生物質の効力は間質性肺炎のマウスのモデルで調査された。感染の後に, マウスは3日間、毎日ドキシサイクリンの単一の投与量かazithromycinの単一の投与量で扱われた。もはや有機体を培養することはできなかったときのどちらかの処理の後に, 感染は排除されるように見えた。しかしながら, 影響を与える投与量によって, 25%か77%のマウスの肺にPCR孤立でC.肺炎 DNAを検出することができるだろう。どんな違いも扱われて, 無処置マウスの肺で観測されなかった。これらの結果は, 単一の投与量処理養生法とその後長期間の処置が必要だったかもしれない後に有機体が固執することができるということを示す。
<介入の研究>
動物のモデル
抗菌性エージェントがいる介入が病気進行を変更することができるかどうか決定することと成功している処理養生法を確認することによって、C.肺炎感染とアテローム性動脈硬化症の動物のモデルはさらに役割を定義する。 ニュージーランドホワイトウサギは食事が0.25%のコレステロールで供給されて, C.肺炎で3回intranasallyに予防接種をされた。 感染したウサギとコントロールは7週間azithromycinで扱われた。 最終的な接種の3カ月後に, 増加する胸部大動脈における最大限の内膜の厚み(MIT)はウサギを感染させたが, コントロールでは感染していなかった。 azithromycinによって扱われたウサギのMITは無処置感染したウサギでそれよりも少なくて, コントロールのものと同様だった。しかしながら, 有機体はそれが無処置ウサギの大動脈に検出されたのと同じくらい頻繁に扱われたウサギの大動脈の免疫蛍光によって検出された。
ヒトの研究
C.
肺炎に対する抗生物質の潜在的使用に関する3つの小さいパイロット研究が有望な結果をもたらした。最初の介入研究は心筋梗塞の少なくとも6カ月後の男性の患者に焦点を合わせた。Titersは血清陰性として任意に分類されるか、介在して陽性であるか、または非常に陽性だった。血清抗体を持っていた人々、3ヶ月後にも保たれたそれが1で扱われたazithromycinの2つのコース(1日あたり500m、経口で3日間)扱われた患者には、心臓血管eventsの五倍の減少と免疫グロブリン(Ig)G測定濃度の減少があった。2
番目の研究は不安定狭心症で入院している202人の患者か非q波の梗塞を含んだ。患者の半分が偽薬(プラセボ)を受けながらロキシスロマイシン(30日間の1日に二度150mg)と他の半分を受けている状態で, 研究はランダマイズされた。血清学は研究における封入か除外のために考慮されなかった。30日後に, 心臓血管eventsの統計的に重要な減少は扱われた患者で観測されたが, 激しい再帰的な狭心症, 急性の心筋梗塞, または虚血性死の結合した終末点がだったときにだけ偽薬を受ける人々が扱われた。3
番目の研究(ランダマイズされる)で, 経皮的冠状動脈の血管再生手順をもっている88人の患者がazithromycin(2日間の1日あたり500mgと28日間の1日あたり250mg)で扱われたか, または偽薬を受け取った。 6カ月後に, azithromycinを受ける患者は偽薬(60%)を受け取る患者よりも血管造影的に確認された再狭窄(9%対16%)と再帰的な狭心症(40%)の両方の下側の頻度を持っていた。抗体titersにおけるどんな変化もazithromycin処理の後に観測されなかった。アステローム性動脈硬化症への研究制限と抗生物質の抗炎症性効果にもかかわらず, 結果は励みになって, より長い観測時間で入念に設計されたより大きいスケールでの介入研究を保証する。
<結論>
心臓血管病における
C.肺炎感染の原因的の役割はまだしっかり確立されていない。 しかしながら、比較で通常の組織において人間のアテローム硬化型組織で見つけられる高頻度の感染; 誘導と進行; アテローム動脈硬化の感染した動物のモデルにおけるアテローム硬化型のような炎症性の変化、人間での抗クラミジア介入研究からの前の結果は病気の過程でC.肺炎の原因の役割と一致している。(
ここまで波多江龍信訳)
-back-